Moderna se dispara en la Bolsa tras solicitar autorización para su vacuna

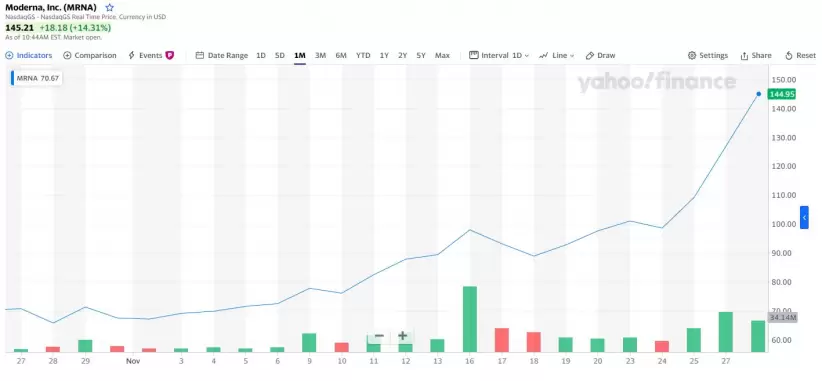
La estadounidense Moderna presentará hoy autorización de emergencia para su vacuna contra el COVID-19 en Estados Unidos y en Europa, luego de que confirmara una eficacia del 94,1 por ciento. Tras este anuncio, las acciones de Moderna reaccionaron con nuevas subidas, “incluso superiores a los dobles dígitos en Wall Street, hasta alcanzar niveles próximos a los US$ 140s por acción”, según el diario español Expansión.
Su éxito en las diferentes fases de prueba de la vacuna llevó a Moderna a multiplicar por seis su cotización en lo que va del año. De hecho, el viernes pasado pasó la barrera de los US$ 50.000 millones de capitalización, unos 41.700 millones de euros.
Las subidas próximas al 10% de hoy representan ganancias adicionales cercanas a los US$ 5.000 millones.
Dos semanas después de haber anunciado una eficacia de 94,5% sobre la base de resultados preliminares, Moderna reportó que de 196 participantes en su ensayo clínico que se infectaron con COVID-19, 185 pertenecían al grupo placebo y 11 al grupo vacunado, con una eficacia calculada de 94,1%.
Esto significa que las personas vacunadas vieron reducido su riesgo de contraer COVID-19 en un 94% en comparación con las personas que no fueron vacunadas, una eficacia similar a la de la vacuna de Pfizer/BioNTech (95%).
Ninguna forma grave de la enfermedad se registró en el grupo vacunado, contra 30 en el grupo placebo, consignó una agencia de noticias. Moderna informó que no se observaron nuevos efectos secundarios graves en los voluntarios vacunados, pero no dijo explícitamente si se observaron inicialmente efectos secundarios graves.
El 16 de noviembre, la compañía anunció que la vacuna era "generalmente bien tolerada" y no había suscitado "preocupaciones de seguridad importantes". Las reacciones más frecuentes no fueron graves, como dolor alrededor del lugar de la inyección en el brazo, fatiga, rigidez muscular o dolor de cabeza. Un participante del ensayo clínico murió, pero estaba en el grupo de placebo.
Moderna informó que la eficacia observada de su vacuna fue uniforme según la edad, el género y la etnia. "Este análisis positivo preliminar confirma la capacidad de nuestra vacuna para prevenir el COVID-19 con una eficiencia del 94,1% y, significativamente, la capacidad para prevenir la forma grave de COVID-19", dijo Stéphane Bancel, el director ejecutivo de Moderna.
La compañía presentará lo que se denomina en Estados Unidos una solicitud de autorización de emergencia a la Agencia de Medicamentos (FDA), que se espera convoque a su comité asesor sobre vacunas el 17 de diciembre. Esto podría permitir, en caso de que sea aprobada, una distribución en los días siguientes. También presentará una solicitud de uso condicional a la Agencia Europea de Medicamentos (EMA).