¿Puede un medicamento ser un privilegio de US$ 2 millones?
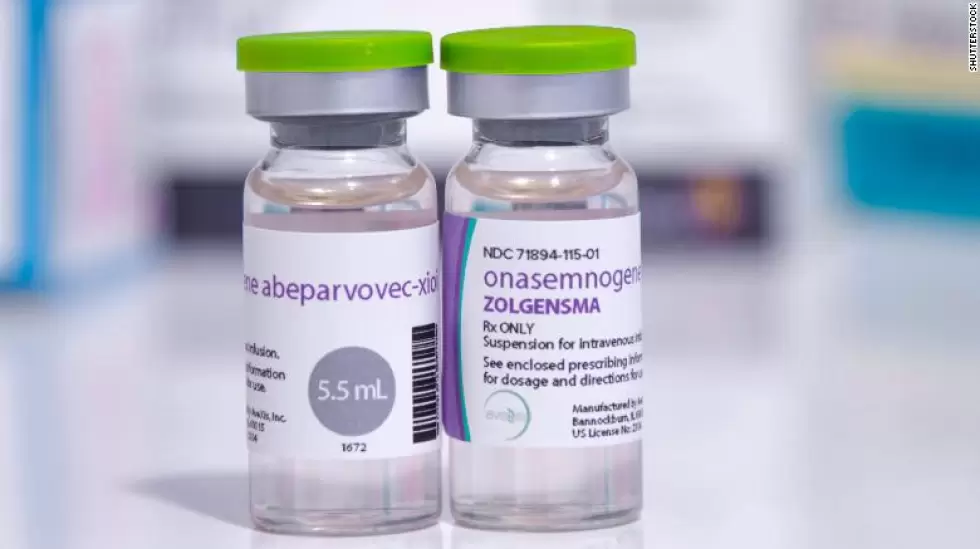
Probablemente, en los últimos días una enfermedad como la Atrofia Muscular Espinal (AME) se haya hecho más conocida para el común de la gente a través del caso de Emma, la beba que necesitaba de Zolgensma, un medicamento de US$ 2 millones que debía adquirir en Estados Unidos para que su patología no avance.
La AME es de las llamadas "enfermedades huérfanas" que afectan a un número muy pequeño de la población y se manifiesta cuando el gen llamado SMN1 no fabrica suficiente cantidad de una proteína que necesitan las neuronas motoras para funcionar con normalidad, las neuronas motoras se descomponen y no pueden enviar mensajes a los músculos. “Se traduce en que progresivamente se pierde la fuerza física necesaria para gatear, andar, sentarse, caminar, comer y respirar”, contaban los padres de Emma a través de las redes y el sitio web que crearon para recaudar los fondos necesarios para comprar el medicamento, su principal escollo.
Lo que le ocurrió a Emma Gamarra y que pudo sortear gracias a la ayuda del influencer Santiago Maratea, quien se puso al hombro la campaña a través de las redes sociales e hizo real lo imposible, que era reunir esa millonaria suma, hoy es muy habitual para aquellas personas que sufren de enfermedades denominadas raras, y cuyos medicamentos son prácticamente inalcanzables.
Esto pone en la mesa el debate sobre la accesibilidad a este tipo de tratamientos y su alto valor cuando solo afecta a porciones minoritarias de la sociedad.
Tras su aprobación, en 2019, Zolgensma se convirtió en el medicamento más caro del mundo. Hace algún tiempo atrás Bloomberg publicó un artículo titulado 'Ningún medicamento milagroso debería costar US$ 2,1 millones'. Allí, no sólo se cuestionaba éticamente el precio, también se cuestionaba al laboratorio Novartis, la multinacional farmacéutica el precio de comercialización.
Es que muchos laboratorios, dedicados a desarrollos basados en terapia génica, aducen que los altos costos están directamente relacionados a una alta inversión previa en I+D que deben recuperar rápidamente. Sin embargo, Novartis no investigó ni desarrolló Zolgensma, sino que adquirió AveXis (su fabricante) por un precio que Novartis recuperará en un plazo relativamente corto”, explicaba el médico Peter Bach.
Además, están aquellos laboratorios que se dedican exclusivamente al tratamiento de "enfermedades raras", que dan cuenta que su negocio es más acotado que aquellos que producen medicamentos para enfermedades crónicas, dado que tienen un "consumidor cautivo" que sostiene el negocio y le posibilita amortizar la inversión previa en el desarrollo de esos medicamentos.
Por otro lado, está la respuesta de los padres para quienes la vida de sus hijos no tiene un precio alto. Tina Anderson, una estadounidense cuyo hijo cumplirá cuatro años de edad gracias a Novartis, sostuvo que el precio que pagaron por el medicamento era justo en comparación con la alternativa: pagar toda una vida por atención domiciliaria, respiradores y hospitalizaciones. A su vez, remarcaban que sin el incentivo de una ganancia, los laboratorios no buscarían una cura.
Familias AME Argentina, una organización que agrupa a familias y pacientes afectados por la enfermedad anunciaba con felicidad algunos días atrás que la ANMAT había concluído el proceso de registro del Zolgensma para el tratamiento de la enfermedad en el país, con la aprobación de comercialización.
Además, explicaron que “estos desarrollos requieren cada vez más inversiones y son de altísimo riesgo. En las moléculas ya conocidas, la tasa de éxito general es baja ya que, de cada 10.000 moléculas que se investigan, solo una llega al mercado. Esta cifra puede ser aún menor en las terapias de avanzada”.
Los laboratorios -agregaron- “necesitan recuperar sus inversiones para continuar investigando y desarrollando nuevos tratamientos” ya que “de otra forma la investigación no es sostenible”. Desde CAEME manifestaron que las terapias avanzadas representan un desafío para lograr un acceso sustentable y que representarán un cambio de paradigma para establecer nuevos esquemas de financiamiento, que se irán adecuando y modificando para cada caso.
Desde la Cámara Argentina de Especialidades Médicas (CAEME) se refirieron al debate ético que se generó en torno al valor que tiene el tratamiento. “Las terapias avanzadas representan un cambio de paradigma para abordar enfermedades. Lo innovador de algunas de estas terapias -como algunas génicas- es que con una única dosis el paciente recibe la totalidad del valor del medicamento. Desde el punto de vista del paciente, el valor terapéutico es indudable, ya que condiciones que provocan enfermedades crónicas que requieren medicación de por vida tienen el potencial de curarse con la aplicación de ese nuevo tratamiento o medicamento”, expresaron.
“Sin dudas no habrá un único modelo de acceso. El precio de un medicamento o tratamiento es un tema complejo, que no puede abordarse de manera liviana, sino que por el contrario requiere un abordaje multidimensional por la totalidad de los actores de los sistemas sanitarios de cada país y el contemplar horizontes de tiempo que incluyan el impacto de las terapias de avanzada”, precisaron desde la entidad.

Previo a la reciente llegada del Zolgensma, el Gobierno nacional estableció un precio máximo de venta del principio activo Nusinersen (Spinraza®) de 12mg/5mL para el tratamiento del AME. La medida había sido resulta por la Secretaría de Comercio Interior, decretaba la baja del costo de un tratamiento estándar de tres años de U$S 1,3 millones a 324.000 dólares.
En 2016, la FDA, el organismo que autoriza y regula el mercado de medicamentos y alimentos en Estados Unidos, aprobó el principio activo Nusinersen del laboratorio Biogen S.R.L. para el tratamiento de AME, en tanto, en la ANMAT fue registrado en 2019 con validez por un año y con la condición de realizar un programa de seguimiento de la evolución de los pacientes.
En mayo de 2019, el Ministerio de Salud firmó un convenio con ese laboratorio que incluía un descuento del 40% para quienes adherían al convenio y que exigía incorporar el medicamento al Programa Médico Obligatorio (PMO). A juicio de las actuales autoridades de esa cartera, ese convenio tenía dos problemas, uno de ellos "una cláusula de confidencialidad por la que no se conocía el precio que se pagaba".
Pero, además, fuentes del Ministerio de Salud indicaron que "el PMO se deben incluir las prestaciones de alta frecuencia, pero no las prestaciones de baja frecuencia y alto costo, que deben estar en un programa especial". Según el Ministerio, haber incluido el medicamento en el PMO "fue disfrazar de acceso lo que no fue, porque las familias debían hacer juicio para que se les diera acceso a los medicamentos, los jueces concedían el amparo y las obras sociales no lo podían pagar".
En junio de 2020 pasado, la ANMAT reinscribió este principio activo en el registro de especialidades medicinales, pero solo para AME 1 y 2 "al no contar con la evidencia que evalúe la eficacia, efectividad y seguridad de esta medicación". El paso siguiente del ministerio de Salud fue rescindir el convenio con Biogen y solicitar a la Secretaría de Comercio Interior que fije un precio máximo, tomando como referencia el valor de la droga en el mercado brasileño. En consecuencia, el principio activo fue eliminado del PMO, pero garantizando la cobertura para todos los pacientes de AME 1, 2 y 3.